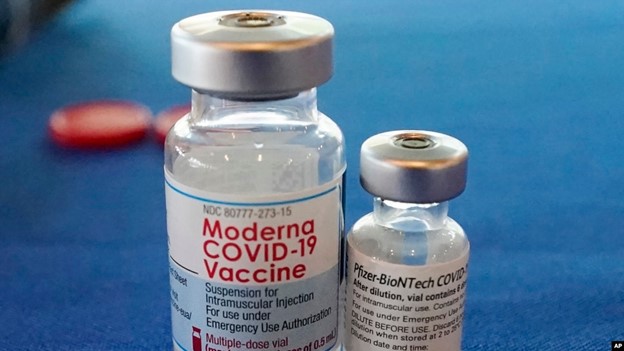
La Administración de Alimentos y Medicamentos de Estados Unidos, (FDA), autorizó el miércoles las inyecciones de refuerzo contra el COVID-19 rediseñadas de Moderna y Pfizer/BioNTech, contra las subariantes ómicron BA.4/BA. 5.
Atlanta, EEUU — La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) autorizó el miércoles las vacunas de refuerzo contra el COVID-19 rediseñadas de Moderna y Pfizer/BioNTech que se dirigen a las subvariantes ómicron BA.4/BA. 5, actualmente dominantes en las infecciones de coronavirus.
Ambas vacunas también incluyen la versión original del virus objetivo de todas las inyecciones anteriores contra el COVID-19, mientras que el país se prepara para otra campaña de vacunación en la temporada del otoño boreal, informa la Voz de América.
En dosis única, la vacuna de Moderna MRNA.O está autorizada para mayores de 18 años, mientras que el candidato bivalente de Pfizer es para mayores de 12 años.
El gobierno de Estados Unidos ha comprado 175 millones de dosis de las vacunas de refuerzo con el fin de evitar los peores efectos de un posible aumento de nuevas infecciones, a medida que las escuelas reabren tras el verano boreal y las personas pasan más tiempo en interiores por las bajas temperaturas.
En junio, la FDA solicitó a los fabricantes de vacunas que adaptaran las inyecciones a las dos subvariantes responsables del aumento más reciente de infecciones en todo el mundo. La subvariante BA.5 actualmente representa más del 88 % de las infecciones en Estados Unidos.
El panel asesor de vacunas de los Centros para el Control y la Prevención de Enfermedades de Estados Unidos (CDC) tiene previsto reunirse el jueves para emitir recomendaciones sobre el uso de refuerzos rediseñados que su directora Rochelle Walensky tendrá en cuenta antes de tomar una decisión final.






